Gdy słyszymy „polimery”, myślimy zazwyczaj o plastiku. Tymczasem to znacznie szersza kategoria – bez polimerów nie byłoby ani papieru, ani wełnianych swetrów, ani nawet życia, bo DNA też jest polimerem! W chemii polimer oznacza długi łańcuch powtarzających się elementów – jakby jedna cząsteczka została powielona setki, tysiące czy miliony razy i połączona w sznur. Krótko mówiąc: polimery otaczają nas zewsząd, w naturze i w wytworach człowieka. Czasami nawarstwiają się w górach śmieci, innym razem otwierają drogę do przełomowych technologii – na przykład w medycynie.
Dobrym przykładem są plastry nikotynowe. Cienki skrawek tworzywa dostarcza substancję psychoaktywną przez skórę prosto do krwiobiegu. Gdyby opowiedzieć o nich naszym dziadkom, najpewniej uznaliby to za abstrakcję, dziś to zwykły zakup w aptece za kilkadziesiąt złotych.
Podobnie w niedalekiej przyszłości możemy patrzeć na „inteligentne” leki – systemy, które same decydują, ile substancji podać i w jakim momencie. Mogą to być tabletki, plastry czy implanty, niewymagające już od pacjenta codziennych pomiarów i samodzielnego dawkowania. Taką możliwość otwierają elektroaktywne materiały mikrożelowe, opracowane niedawno przez chemików z Uniwersytetu Warszawskiego.
Mikrożelowa mikrohistoria
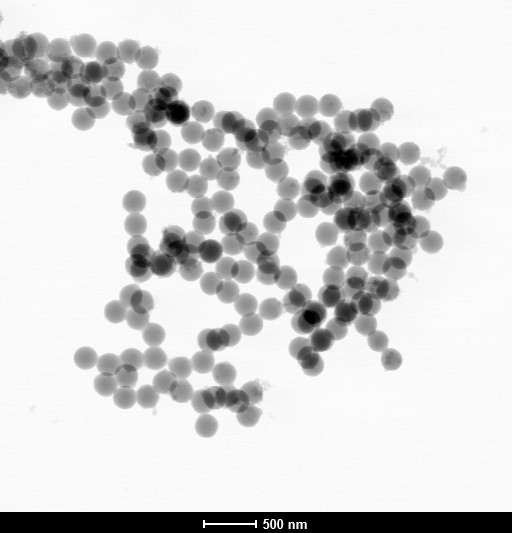
Mikrożele polimerowe nie są nowym odkryciem – naukowcy pracują nad nimi od lat. Klucz tkwi jednak w tym, jak nadać im odpowiednie właściwości. W największym skrócie to mikroskopijne, kuliste struktury zbudowane z sieci polimerowych. Mogą wchłaniać różne substancje – na przykład leki – a następnie stopniowo je uwalniać.
Zespół z Wydziału Chemii UW, kierowany przez dra Kamila Marcisza, opracował mikrożel o cechach, które wyróżniają go na tle dotychczasowych rozwiązań. Jest niezwykle plastyczny – potrafi zmieniać rozmiar i wracać do pierwotnej formy. Reaguje zarówno na temperaturę, jak i na sygnał elektryczny. Co więcej, może uwalniać zgromadzoną substancję w sposób kontrolowany, zależnie od warunków zewnętrznych.
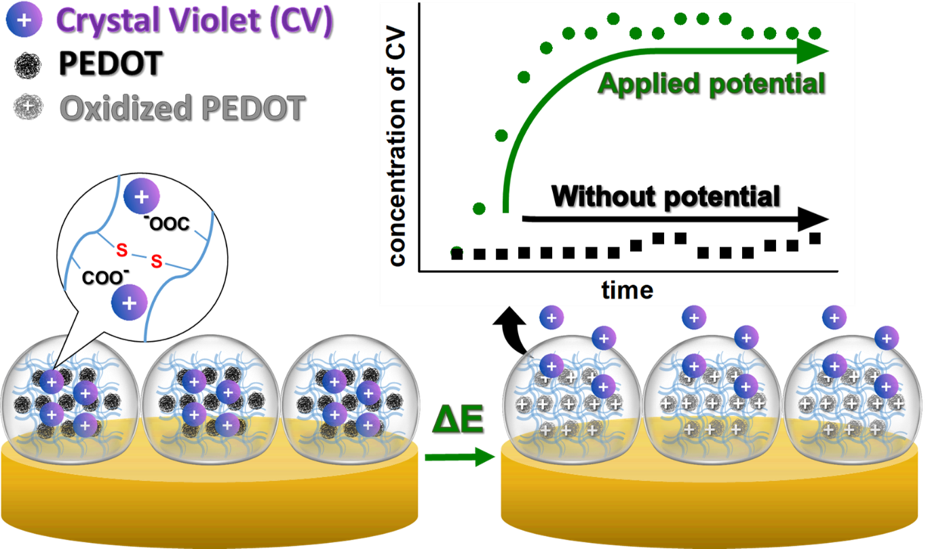
Jak to działa? Opracowany materiał jest kombinacją kilku rodzajów polimerów połączonych w jedną sieć tworzącą mikrożel. Za jego plastyczność odpowiadają termoczułe mikrożele pNIPA – poli(N-izopropyloakryloamid) – oraz polimer przewodzący, a więc reagujący na sygnał elektryczny, PEDOT – czyli poli(3,4-etyleno-1,4-dioksytiofen). Całość osadzono na elektrodzie złotej, która rejestruje impulsy i pozwala sterować zachowaniem materiału.
Aby mikrożel mógł być „wypełniony” substancją aktywną, np. lekiem, i następnie ją uwalniać, potrzebny był jeszcze specjalny łącznik – kwas akrylowy (związek chemiczny zawierający grupy karboksylowe). To on pełni rolę nośnika dla substancji aktywnej. Dopiero taka konstrukcja sprawiła, że udało się uzyskać materiał, który może okazać się przełomowy.
– Dzięki temu możliwa jest regulacja ilości uwalnianej substancji z matrycy mikrożelowej osadzonej na powierzchni elektrody poprzez przyłożenie odpowiedniego potencjału elektrochemicznego. Podsumowując, udało nam się rozwinąć znaną technologię, co poszerzyło zakres jej praktycznych zastosowań i stanowi istotny krok w kierunku konstrukcji implantów wewnątrzustrojowych lub plastrów do przezskórnego transportu substancji, opartych na elektroresponsywnych materiałach hydrożelowych – mówi dr Kamil Marcisz z Wydziału Chemii UW.
Technologia jutra już dziś?
Materiały opracowane na UW nie są zupełnie nowym wynalazkiem, ale wyróżniają się wyjątkową cechą: można je bardzo precyzyjnie kontrolować za pomocą bodźców elektrochemicznych. To już nie tylko powolne, stopniowe uwalnianie leku do organizmu, lecz możliwość regulowania procesu na bieżąco. W praktyce oznacza to, że mikrożel „potrafi” uwalniać dokładnie taką dawkę substancji, jakiej pacjent potrzebuje w danym momencie.
– Różnica pomiędzy obecnie dostępnymi systemami a naszym podejściem polega na tym, że te pierwsze działają głównie pasywnie – uwalnianie substancji aktywnej odbywa się w trybie ciągłym. My poszukujemy rozwiązań, w których uwalnianie leku można aktywnie regulować za pomocą odpowiedniego sygnału elektrycznego. Oznacza to, że pacjent w przyszłości mógłby otrzymać implant lub plaster, który po otrzymaniu sygnału uwalniałby dokładnie taką dawkę leku, jaka jest potrzebna w danym momencie – podkreśla warszawski chemik.
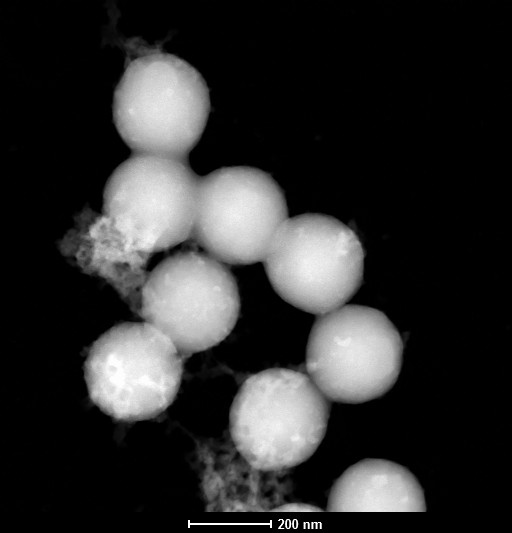
Tym, co najbardziej odróżnia mikrożele od innych materiałów tego rodzaju jest ich plastyczność i rozmiar. Mikroskopijna skala sprawia, że mniej znaczy więcej. Im mniejsza jest taka struktura, tym większa jej powierzchnia w stosunku do objętości. A to oznacza lepszy kontakt z otoczeniem i szybszą reakcję na bodźce.
Hydrożele, z którymi możemy się spotkać dzisiaj mają zazwyczaj wymiary powyżej 1 milimetra. W przypadku mikrożeli, mówimy o skali „mikro”, a więc o kulistej strukturze o średnicy od kilkuset nanometrów do kilkuset mikrometrów. Podczas gdy milimetr to tysięczna część metra, nano oznacza jego miliardową, a mikro – milionową część. Dzięki tym niemal niedostrzegalnym rozmiarom, mikrożele mogą wykonywać zadania, których większe hydrożele nie są w stanie spełnić.
– Hydrożelowe plastry dostępne w aptekach pełnią przede wszystkim funkcję ochronną i nawilżającą – łagodzą ból i przyspieszają gojenie ran. Mikrożele, nad którymi pracujemy, to materiały o znacznie bardziej zaawansowanych właściwościach. Potrafią reagować na bodźce zewnętrzne, takie jak temperatura czy sygnał elektryczny, dzięki czemu mogą zmieniać swoje rozmiary i w sposób kontrolowany uwalniać substancje aktywne – zaznacza uczony.

Pieśń (nieodległej?) przyszłości
Te dwie cechy – zdolność do kontrolowanego uwalniania substancji i elastyczność przy mikroskopijnych rozmiarach – sprawiają, że technologia rozwinięta na UW ma ogromny potencjał.
– Praktyczne zastosowania takich układów dotyczą przede wszystkim medycyny. Głównym celem naszego systemu było opracowanie zaawansowanego mechanizmu dostarczania leków, w którym uwolnienie substancji aktywnej następuje w sposób kontrolowany – mówi dr Marcisz.
To właśnie kontrola jest tu kluczowa. Dzięki niej możliwe staje się stworzenie „inteligentnych” implantów czy plastrów, które nie tylko podadzą lek, ale też same ocenią, jaka dawka jest w danym momencie potrzebna. Można to porównać do odruchu źrenicy w oku – rozszerza się lub zwęża automatycznie, w zależności od ilości światła. Mikrożele mogłyby działać podobnie. Potencjalnie będą służyć także w diagnostyce, jako sensory i biosensory elektrochemiczne, czyli czujniki reagujące na sygnały elektryczne generowane przez organizm lub monitorujące jego stan.
Wyobraźmy sobie, że implant bada poziom glukozy u chorego na cukrzycę. Jeśli poziom rośnie, urządzenie wysyła impuls elektryczny do mikrożelu, a ten uwalnia dokładnie tyle insuliny, ile jest potrzebne, by przywrócić równowagę. W przypadku innych terapii mogłoby to działać podobnie: czujnik wykrywa sygnał biologiczny, a mikrożel reaguje, wypuszczając odpowiednią dawkę leku.
To jednak dopiero początek możliwości. Mikrożele mogą znaleźć zastosowanie nie tylko w medycynie czy farmacji. Ich zdolność do szybkiej zmiany objętości pod wpływem impulsu elektrycznego przypomina działanie naszych mięśni – kurczą się i rozluźniają zależnie od sygnałów nerwowych. Dzięki temu można sobie wyobrazić rolę mikrożeli w robotyce czy protetyce: jako sztucznych mięśni, które pozwolą protezom poruszać się bardziej naturalnie, a robotom wykonywać precyzyjne, płynne ruchy.
– W przemyśle elektroaktywne mikrożele mogą znaleźć zastosowanie w systemach oczyszczania środowiska, analizie wód pod kątem skażeń czy w przemyśle spożywczym – do wykrywania patogenów i toksyn. Ciekawą perspektywą jest również ich wykorzystanie w systemach typu „lab-on-a-chip” [z ang. ‘laboratorium czipowe’, czyli mikroskopijne urządzenie laboratoryjne wykorzystywane w diagnostyce], wyposażonych we wbudowane elementy logiczne, umożliwiające samodzielną analizę próbek i podejmowanie decyzji diagnostycznych – podsumowuje badacz.
Lista potencjalnych zastosowań jest tak długa, że sama może przyprawić o ból głowy. I choć na lek stworzony w oparciu o mikrożele trzeba jeszcze poczekać, wcale nie musi to być odległa perspektywa. W świecie biomateriałów droga od laboratoriów do pierwszych badań klinicznych potrafi zająć kilkanaście lat. Jeśli więc tempo badań się utrzyma, pierwsze „inteligentne” implanty zobaczymy jeszcze zanim obecni studenci chemii zdążą napisać doktoraty.