Choć nie widać tego gołym okiem, pod naszymi stopami tętni życie. Miliony mikroorganizmów współtworzą podstawę działania całych ekosystemów. Mikrobiom gleby, czyli ogół żyjących w niej drobnoustrojów, zasadniczo wpływa na to, jak wygląda obieg składników odżywczych, a także na zdrowie i odporność roślin. Wiedza o tym, jakie bakterie można znaleźć w podłożu, ma więc kluczowe znaczenie dla rolnictwa i inżynierii środowiska – zwłaszcza dziś, gdy intensywne nawożenie czy stosowanie środków ochrony roślin potrafi zaburzać naturalny mikrobiom gleby*, czyniąc rośliny bardziej podatnymi na choroby.
Mimo że naukowcy od lat starają się opisywać mikrobiologiczny skład gleby, to stosowane aktualnie metody, mają duże ograniczenia i wymagają dalszego rozwoju. Tradycyjne techniki badawcze pokazują jedynie część prawdy – ponieważ wychwytują tylko określone grupy bakterii, nie ujawniają pełnej różnorodności mikroorganizmów. Alternatywą były pełne, zaawansowane skany genetyczne, które dostarczają głębszych informacji – lecz ich koszt sprawiał, że trudno było stosować je na większą skalę.
Na ten właśnie problem postanowił odpowiedzieć zespół badawczy z Laboratorium Mikrobiologii Rolniczej i Przemysłowej przy Instytucie Bioinżynierii Wydziału Biologii Uniwersytetu Warszawskiego, działający pod kierunkiem dr Klaudii Dębiec-Andrzejewskiej. Stosując innowacyjną metodę tzw. two-step metabarcoding (TSM), udoskonalającą stosowane obecnie techniki, mikrobiolodzy z UW udowodnili, że badania mikrobiomu gleby można prowadzić nie tylko uzyskując dokładniejsze wyniki, ale też że głębszy wgląd w mikrobiologiczną bioróżnorodność jest możliwy w tańszy i bardziej efektywny sposób.

Zobaczyć więcej
W dotychczasowych badaniach mikrobiomu wykorzystywano zwykle test tzw. sekwencjonowania 16S rDNA, pozwalający odczytywać fragmenty DNA bakterii.
Do analizy używa się w nim uniwersalnych starterów (primerów) – czyli krótkich odcinków DNA, które w praktyce działają jak znaczniki lub „haczyki” przyczepiające się do określonych fragmentów genów bakterii w próbce. Po przyłączeniu startera enzym potrafi powielić ten fragment DNA, dzięki czemu można go następnie odczytać, co pozwala zidentyfikować mikroorganizm.
Uniwersalne startery mają wykrywać jak najszerszy zestaw mikroorganizmów, ale ta wszechstronność powoduje, że część z nich jest nadreprezentowana, a część pomijana. Naukowcy z UW zaproponowali więc, by badanie przeprowadzić dwuetapowo.
Najpierw wykonali klasyczne sekwencjonowanie z użyciem uniwersalnych starterów, aby ogólnie określić skład mikrobiomu. Następnie, dla najliczniejszych grup drobnoustrojów (m.in. Actinobacteria, Acidobacteria, Firmicutes czy Alphaproteobacteria) użyli jeszcze starterów specyficznych, zaprojektowanych tak, aby dokładniej badały wybrane, pomniejsze podgrupy. Te cztery grupy bakterii są szczególnie ważne – odpowiadają za kluczowe procesy w glebie, wspierają wzrost i odporność roślin oraz kształtują obieg składników odżywczych.
Actinobacteria – często występują w glebie, rozkładają martwą materię organiczną i produkują naturalne antybiotyki, wspierając zdrowie roślin. Acidobacteria – bardzo różnorodne, powszechne w glebach kwaśnych, biorą udział w obiegu węgla i składników odżywczych. Firmicutes – niektóre gatunki tworzą przetrwalniki i wspomagają rośliny w walce z patogenami. Alphaproteobacteria – obejmują bakterie symbiotyczne, np. wiążące azot, co pomaga roślinom w pobieraniu tego kluczowego pierwiastka.
Okazało się, że użycie takiej celowanej metody znacznie zwiększa liczbę rodzajów wykrytych mikroorganizmów – nawet wielokrotnie. Na przykład, w przypadku typu Firmicutes tą metodą wykryto 124 ich rodzaje (29 przy starterach uniwersalnych), a przy Alphaproteobacteria – 111 (w porównaniu do 44).
Dodatkowo, naukowcy porównali wyniki z badaniem metagenomowym shotgun – czyli ogólną analizą całego materiału genetycznego gleby, bez użycia starterów. Okazało się, że rezultaty TSM są do niej podobne, a więc dają znacznie mniej zniekształcony, statystycznie wiarygodny obraz mikrobiomu.
– Dzięki temu, że w naszych badaniach schodzimy głębiej, uzyskujemy o wiele lepsze pojęcie o bioróżnorodności obszaru, z którego dana próbka pochodzi. To ważne, bo istnieje bezpośredni związek między zróżnicowaniem występowania bakterii a życiem roślin. Im więcej grup tych pierwszych, tym lepiej, ponieważ rośliny wchodzą z nimi w ścisłą i złożoną współpracę – mówi dr Klaudia Dębiec-Andrzejewska.
Próbki gleby, które analizowali naukowcy z UW, pochodziły z Mazowsza – z pól uprawnych w okolicach Otwocka. Po pobraniu wierzchniej warstwy gleby rolniczej (ok. 30 cm głębokości) zostały dokładnie wymieszane i umieszczone w kontrolowanych warunkach laboratoryjnych.
Przez 120 dni gleba „dojrzewała” w komorze klimatycznej, w stałej temperaturze około 20 °C. Wilgotność ustawiono na 40% maksymalnej pojemności wodnej, czyli ziemia była lekko wilgotna, ale daleka od „przelania”.
Ten długi okres inkubacji nie miał na celu namnażania bakterii, lecz ustabilizowanie mikrośrodowiska – tak, aby mikrobiom osiągnął równowagę i lepiej odzwierciedlał naturalne warunki. Dopiero po takim przygotowaniu zebrano właściwe próbki do analizy chemicznej i sekwencjonowania DNA mikroorganizmów.
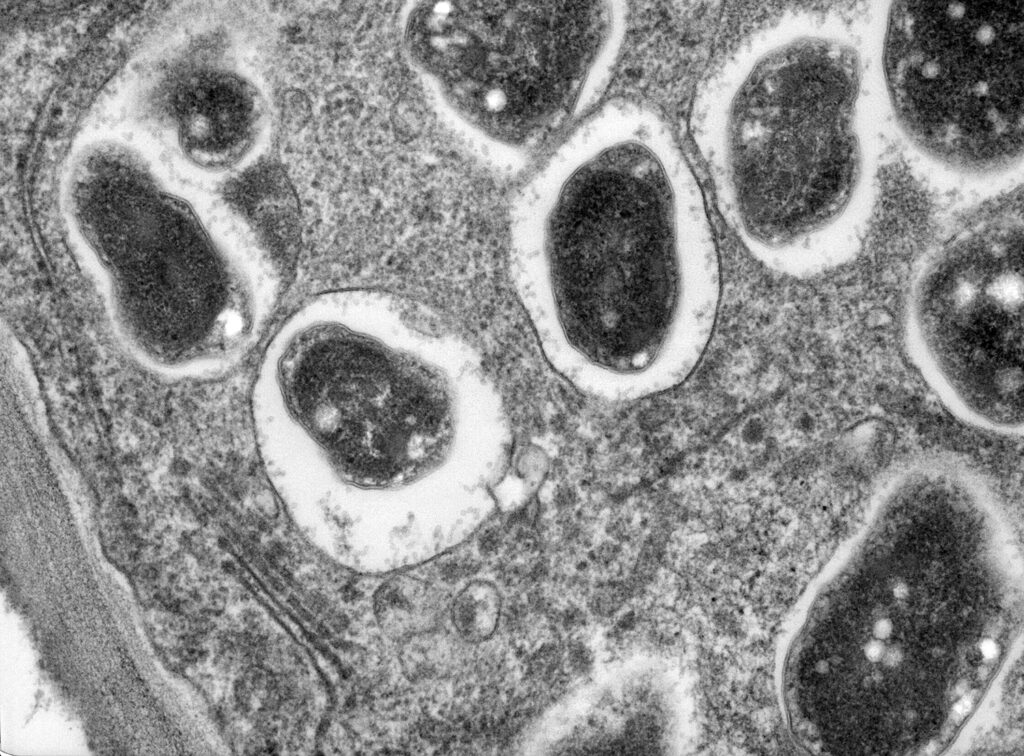
Mikroskopijni pomocnicy
Rośliny nieustannie mierzą się z różnymi wyzwaniami: zmianami temperatury, suszą, niedoborem światła czy atakami szkodników. A jednak w bakteriach mają swoich wielkich sprzymierzeńców. Kiedy roślina musi podjąć walkę z jakimś szkodliwym czynnikiem, wysyła do swojego systemu korzeniowego specjalne substancje, które wabią określone rodzaje tych mikroorganizmów. One zaś wspierają ją w walce z patogenami, na przykład wytwarzając odpowiednie związki chemiczne. Szerszy arsenał bakterii i innych mikroorganizmów w glebie oznacza więc po prostu większą pulę środków obronnych, które rośliny mogą w takich zmaganiach wykorzystać.
– Mimo że nasze badanie ma charakter wyłącznie opisowy, to znaczy nie dodajemy w nim niczego do gleby, co mogłoby jakoś wpłynąć na mikrobiom, to taki opis ma bardzo duże znaczenie sam w sobie. Dzięki niemu wiemy, co kryje w sobie gleba na danym obszarze, a więc również, czy wymaga jakichś, ułatwiających uprawę roślin, ulepszeń – zaznacza dr Dębiec-Andrzejewska.
Ustalenie mikrobiologicznego składu danego podłoża nie musi być końcowym etapem badań. Poprzez interwencję człowieka można modyfikować mikrobiom – zwiększać różnorodność mikroorganizmów czy wspomagać ich aktywność. Może się też okazać, że jest ich tak dużo, że żadna ingerencja nie jest potrzebna. Ta wiedza pozwala z kolei zmniejszyć nakład pracy przy uprawach oraz ich koszt.
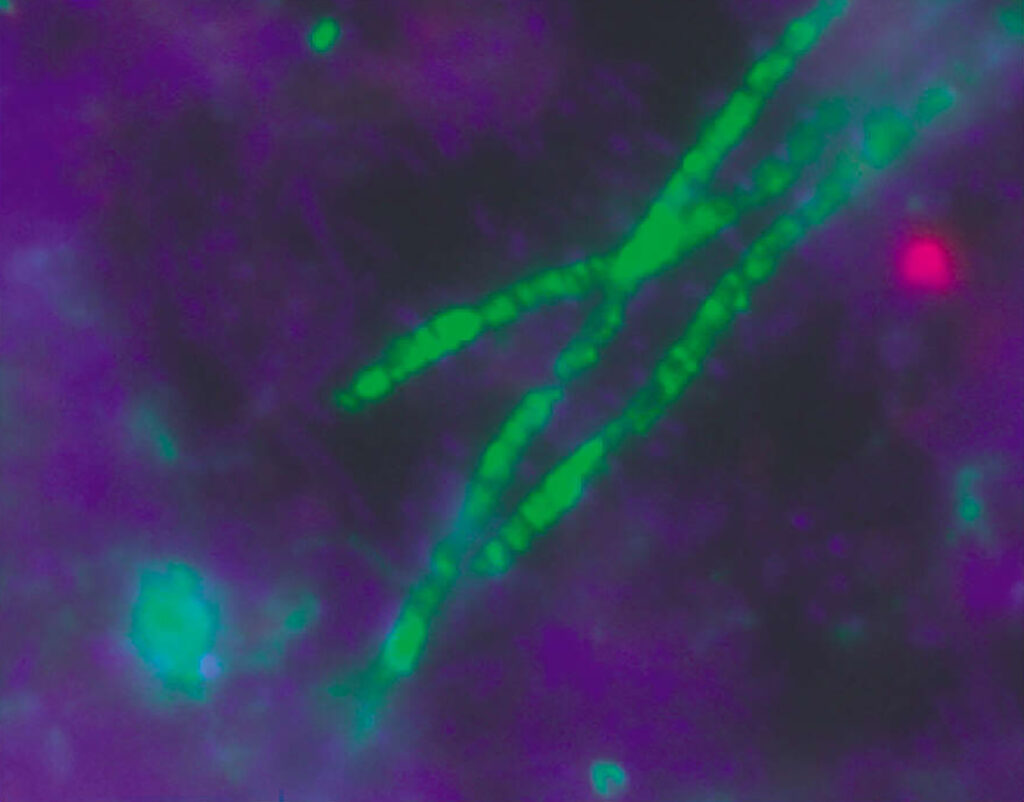
Niedoskonałe radary i zrzuty ekranu
Testy molekularne umożliwiają dziś rozpoznawanie tysięcy grup mikroorganizmów – nie tylko bakterii, ale też np. grzybów czy protistów. I mimo że wiadomo już wiele, to wciąż istnieje szereg ważnych zadań, przed którymi stoją mikrobiolodzy.
Przede wszystkim, stosowane rutynowo metody pokazują zaledwie część rzeczywistej bioróżnorodności. Mikroorganizmy glebowe tworzą rozbudowane sieci zależności, które wpływają na obieg pierwiastków, dostępność składników odżywczych, stabilność środowiska oraz zdolność ekosystemów do reagowania na zmiany. Nawet niewielkie różnice w składzie mikrobiomu mogą przekładać się na istotne zmiany funkcjonowania całych systemów biologicznych. Z tego względu coraz większą wagę przykłada się nie tylko do obecności pojedynczych grup mikroorganizmów, lecz także do ich różnorodności, wzajemnych relacji oraz zmienności w czasie i przestrzeni.
Co więcej, testy, które stosujemy najczęściej, w pewnym sensie pozwalają na wykrycie tylko powierzchownego obrazu. Skoro bakterie są „namierzane” na podstawie sygnałów pochodzących z ich materiału genetycznego, badanie najłatwiej ujawnia obecność tych grup, które występują najliczniej i dominują w danym środowisku. Mikroorganizmy rzadkie, niszowe lub obecne w niewielkich ilościach mogą pozostawać w tle, a ich udział w funkcjonowaniu ekosystemu gleby bywa trudny do uchwycenia.
Możliwe więc, że istnieją duże grupy mikroorganizmów, których do tej pory taki radar w ogóle nie wychwycił, a ich rola w ekosystemach może być znaczna. Ciekawe zresztą, że samo pojęcie gatunku okazuje się w przypadku bakterii problematyczne, dlatego w badaniach nad bioróżnorodnością mikrobiologiczną coraz częściej akcentuje się znaczenie szerszych jednostek oraz podejścia systemowego, które pozwala uchwycić pełniejszy obraz życia mikrobiologicznego.
– W mikrobiologii wolimy posługiwać się szerszym pojęciem – rodzaju, który jest wyższą niż gatunek jednostką klasyfikacji organizmów. Chodzi o to, że bakterie charakteryzuje ogromna zmienność. Wystarczy, że warunki się trochę zmienią, a one już będą się do nich przystosowywać, mutując. Dlatego w żargonie o takich opisach mówimy, z przymrużeniem oka, „zrzut ekranu” – to jak stan pogody, rejestracja bieżącej chwili. Gdy jednak zostawiamy próbkę na tydzień, to nigdy nie wiemy, do czego wrócimy – mówi dr Dębiec-Andrzejewska.

Bakterioterapia gleby i plonów
Dzięki zastosowaniu metodologii two-step metabarcoding naukowcy z UW pokazali, że możliwe jest bardziej efektywne i precyzyjne poznawanie złożonego świata mikroorganizmów glebowych. Metoda ta stanowi jedno z narzędzi, które mogą okazać się szczególnie przydatne w badaniach nad strukturą i funkcjonowaniem mikrobiomu gleby. Tego typu wiedza jest istotnym krokiem w kierunku lepszego zrozumienia procesów zachodzących w ekosystemach rolniczych i może w przyszłości stanowić podstawę do opracowywania bardziej zrównoważonych, mniej inwazyjnych praktyk rolniczych, choć jej praktyczne wykorzystanie wymaga jeszcze dalszych badań i weryfikacji.
Zespół dr. Klaudii Dębiec-Andrzejewskiej i współpracowników podjął się kolejnego kroku – przeniesienia wyników badań z laboratorium do praktyki. W 2023 r. powstała spółka spin-off UW – BHUMI, która pracuje nad biopreparatami i bionawozami dla rolnictwa – substancjami opartymi na komórkach bakterii i grzybów albo na ich metabolitach (np. sideroforach), stanowiących naturalny sposób wspierania gleby.
Preparaty te, mogą pomóc w odbudowie zdrowego mikrobiomu gleby, zwiększyć bioróżnorodność mikrobów korzystnych dla roślin, poprawić dostępność składników pokarmowych (takich jak żelazo, fosfor) oraz zmniejszyć potrzebę stosowania chemicznych nawozów czy środków ochrony roślin. Dzięki temu rolnictwo mogłoby być bardziej przyjazne dla środowiska, a jednocześnie – bardziej odporne na zmienne warunki klimatyczne.