Współczesna medycyna, biologia i chemia rozwijają się tak dynamicznie, bo coraz lepiej możemy „podglądać” mikroświat. Mikroskopy działają dzień i noc zbierając tysiące, miliony danych eksperymentalnych. Człowiek już dawno nie jest w stanie analizować i interpretować wyników tych pomiarów „ręcznie” – potrzeba nie tylko szybkich komputerów, ale przede wszystkich sprytnych algorytmów, które poradzą sobie nie tylko z terabajtami danych, ale i z niepewnością pomiarową mikroświata.
Spektrometria i spektroskopia – jak to działa?
Współczesna nauka potrafi zajrzeć głęboko w materię – aż do poziomu pojedynczych cząsteczek, których rozmiar mierzy się w nanometrach (miliardowych częściach metra). Takie obiekty można zobaczyć za pomocą mikroskopu elektronowego.
Poznanie dokładnego składu przeróżnych substancji oglądanych pod mikroskopem – leków, płynów ustrojowych, tkanek, lub sztucznie wytworzonych polimerów jest możliwe między innymi dzięki spektrometrii mas i spektroskopii magnetycznego rezonansu jądrowego – dwóm relatywnie skomplikowanym, choć używanym już od dawna, technikom analitycznym.
Techniki te wykorzystują różne w swej naturze zjawiska fizyczne. Spektrometria mas „podgląda” odchylanie jonów w polu elektrycznym, a spektroskopia rezonansu jądrowego – proces absorpcji energii fal radiowych przez jądra atomów umieszczonych w silnym polu magnetycznym.
Spektrometria mas pozwala ustalić, z czego zbudowana jest próbka i w jakich proporcjach występują poszczególne składniki. Atomy i cząsteczki są w niej jonizowane, czyli przekształcane w cząstki naładowane, a następnie rozpędzane w polu elektrycznym. W zależności od masy i ładunku jony poruszają się z różną prędkością, tworząc charakterystyczny wzór – coś w rodzaju chemicznego kodu kreskowego, z którego można odczytać skład próbki. Taki zapis nazywany jest widmem, a jego analiza pozwala zidentyfikować obecne w próbce substancje oraz określić ich ilościowy udział.
Spektroskopia magnetycznego rezonansu jądrowego pozwala z kolei zajrzeć w strukturę cząsteczek. Technika ta śledzi, jak jądra atomów reagują na fale radiowe w silnym polu magnetycznym. Każdy rodzaj atomu np. węgla czy azotu – reaguje w nieco inny sposób, wysyłając sygnał o charakterystycznej częstotliwości.
Jak analizować miliony informacji?
W obrazowaniu spektrometrycznym, w którym badany jest skład przestrzenny tkanki, każdy piksel zawiera informację o tysiącach metabolitów i peptydów znajdujących się w danym miejscu. Metabolity to produkty przemian biochemicznych (metabolizmu) zachodzących w organizmie.
Trudna jest też analiza widm magnetycznego rezonansu jądrowego leków, które składają się z kilku lub kilkunastu substancji czynnych i pomocniczych. Podobnych problemów nastręczają syntetyczne polimery, zawierające łańcuchy o różnych długościach i różnych grupach bocznych.
Niemniej w każdym z wymienionych przykładów uzyskane dane pomiarowe można analizować za pomocą podobnych metod – algorytmów wysokoprzepustowych, działających na gigabajtach danych wygenerowanych z pojedynczego eksperymentu.
Algorytmy uczą się dziś tłumaczyć język mikroświata na zrozumiałe informacje.
Jak zamienić chemię w równania
Każdy eksperyment generuje gigabajty danych, których interpretacja wymaga wsparcia komputerów. Dlatego w laboratoriach coraz większą rolę odgrywa informatyka.
Głównym zadaniem dla informatyka wchodzącego do laboratorium chemicznego albo biologicznego, jest zidentyfikowanie substancji znajdujących się w próbce i oszacowanie proporcji składników.
Widmo badanej substancji można wyobrazić sobie jako ciąg słupków ułożonych obok siebie na osi liczb – na wykresie. W widmie masowym położenie słupka odpowiada masie substancji, a jego wysokość – intensywności sygnału. Im bardziej złożona jest badana mieszanina, tym więcej sygnałów się nakłada – tym więcej niejednoznaczności pojawia się w widmie, a to oczywiście utrudnia analizę, trudniej odczytać, co naprawdę kryje się w próbce.
Badacze z grupy prof. Anny Gambin z Wydziału Matematyki, Informatyki i Mechaniki UW we współpracy z grupą prof. Krzysztofa Kazimierczuka z Centrum Nowych Technologii UW zaproponowali algorytm, który porównuje widma, używając pojęcia optymalnego transportu.
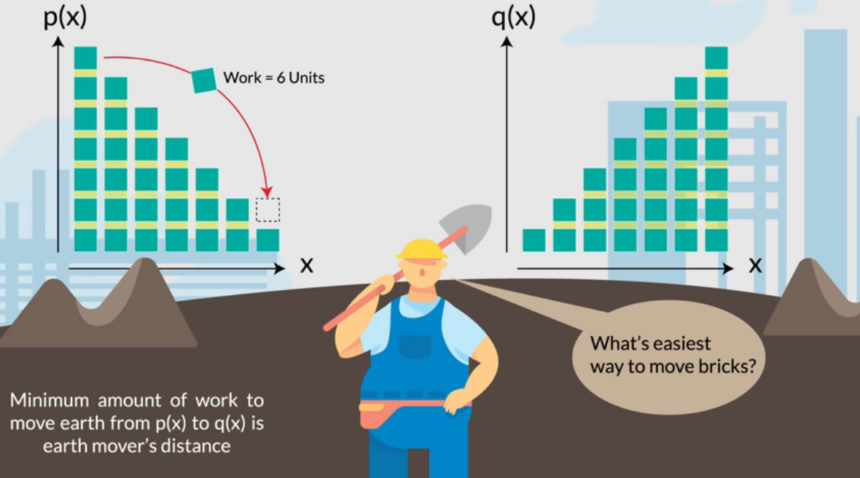
– Optymalny transport można opisać jako przekształcanie górki piasku w inną górkę piasku o zadanym kształcie. Zadanie jest takie, żeby zmienić kształt górki na nowy, przenosząc piasek i wykonać przy tym jak najmniej pracy. Praca jest liczona jako masa przenoszonego piasku razy odległość, na jaką piasek jest przenoszony. Można znaleźć sposób przenoszenia piasku (plan transportowy), przy którym wykonana praca będzie minimalna. Ta minimalna praca to odległość Wassersteina między górkami piasku – tłumaczy Barbara Domżał, doktorantka zajmująca się rozwijaniem metod algorytmicznych do analiz spektroskopowych.
Magnetstein
Na tej koncepcji badacze z Uniwersytetu Warszawskiego wypracowali algorytm nazwany Magnetstein. Wykorzystuje on zasadę optymalnego transportu, by jak najdokładniej porównywać widma uzyskane w różnych eksperymentach.
Nazwa algorytmu nie jest przypadkowa: łączy słowo magnet – nawiązujące do magnetycznego rezonansu jądrowego – z członem stein od nazwiska rosyjskiego matematyka Leonida Wassersteina, od którego nazwano stosowaną tu odległość Wassersteina, która jest wykorzystywana do porównywania widm.
Wykrywanie chorób i projektowanie leków
Badania naukowców z UW i opracowany na Uniwersytecie Warszawskim algorytm mogą znaleźć zastosowanie w metabolomice – dziedzinie badającej procesy przemiany materii w organizmach żywych. Dzięki niemu można analizować procesy metaboliczne, wykrywać zaburzenia enzymatyczne czy identyfikować biomarkery, czyli wskaźniki sygnalizujące predyspozycje lub obecność choroby w organizmie.
Dla bioinżynierów i chemików projektujących leki Magnetstein może mieć znaczenie przełomowe. Pozwala bowiem precyzyjne określać stężenia metabolitów i innych związków chemicznych w próbkach biologicznych oraz w mieszaninach reakcyjnych.
– Ilościowa spektroskopia magnetycznego rezonansu jądrowego służy także do monitorowania działania leków, oceny ich toksyczności i indywidualnej reakcji organizmu, a także do badania wpływu diety, mikrobiomu i czynników środowiskowych na metabolizm. W projektowaniu leków metoda wspiera optymalizację syntez, ocenę czystości substancji czynnych oraz ilościową analizę metabolitów leków, a także badanie oddziaływań białko-ligand, co pomaga w selekcji i optymalizacji kandydatów na leki – doprecyzowuje Barbara Domżał.
Prawidłowa identyfikacja markerów chorobowych ma pomóc lekarzom w trafniejszym diagnozowaniu chorób, takich jak cukrzyca, nowotwory czy schorzenia neurodegeneracyjne. A dla inżynierów farmaceutycznych dokładne poznanie składu chemicznego mieszanin to najpotężniejsze narzędzie w walce o to, by stworzyć skuteczny lek.